| Titel: | Neue Verfahrungsweisen zur Bestimmung des Werthes der Potasche und Soda, der Säuren und des Braunsteins; von Dr. R. Fresenius und Dr. H. Will. |
| Fundstelle: | Band 90, Jahrgang 1843, Nr. XXXII., S. 126 |
| Download: | XML |
XXXII.
Neue Verfahrungsweisen zur Bestimmung des Werthes
der Potasche und Soda, der Saͤuren und des Braunsteins; von Dr. R. Fresenius und Dr.
H. Will.Wir entnehmen diese Abhandlung den Annalen der Chemie und Pharmacie,
Juliusheft 1843. Um ihre Pruͤfungsmethoden fuͤr
Alkalien, Saͤuren, Braunstein etc., welche sich durch leichte
Ausfuͤhrbarkeit und große Genauigkeit auszeichnen, dem groͤßeren
chemischen Publicum zugaͤnglicher zu machen, haben die Verfasser die
Begruͤndung dieser Methoden, die Anfertigung der Apparate, die
Ausfuͤhrung der Operationen, die Berechnung und zwekmaͤßigste
Darstellungsweise der Resultate ausfuͤhrlich und leicht faßlich in einer
besonderen Schrift beschrieben, welche den Titel fuͤhrt: „Neue Verfahrungsweisen
zur Pruͤfung der Potasche und Soda, der Aschen, der
Saͤuren, insbesondere des Essigs so wie des Braunsteins auf ihren
wahren Gehalt und Handelswerth, fuͤr Chemiker, Pharmaceuten,
Techniker und Kaufleute lediglich nach eigenen Versuchen
bearbeitet von Dr. R.
Fresenius und Dr. H. Will, Assistenten am chemischen
Laboratorium zu Gießen. Heidelberg, akademische
Verlagshandlung von C. F. Winter,
1843.“Hr. Mechanikus Fuhr in Gießen haͤlt alle zur
Alkalimetrie, Saͤure- und Braunsteinpruͤfung nach diesen
Methoden noͤthigen Apparate (Waagen, Gewichte, Spirituslampen,
Schaͤlchen, Kohlensaͤureapparate u. s. w.), so wie die
erforderlichen Chemikalien (doppeltkohlensaures Natron, neutrales oxalsaures
Natron etc.) vorraͤthig; sie werden sowohl im Ganzen, so wie im Einzelnen
zu billigen, festgestellten Preisen erlassen.A. d. R.
Mit Abbildungen auf Tab.
II.
Fresenius u. Will, neue Verfahrungsweisen zur Bestimmung des
Werthes der Potasche und Soda.
I. Prüfung
der Potasche und Soda auf ihren Handelswerth. — Alkalimetrie.
Die Methoden, welche zum Zweke haben, den Gehalt der Potasche und Soda an Kali und Natron oder vielmehr
an den kohlensauren Salzen dieser Basen zu ermitteln,
werden alkalimetrische Methoden, die Gesammtheit
derselben Alkalimetrie genannt. Die Wichtigkeit der
lezteren für den Handel, ihre Bedeutung für Fabrikanten und Consumenten war die
Veranlassung, daß sich bereits viele Chemiker mit derselben beschäftigt haben. Alle
aber folgten dabei einem und demselben Principe, dem nämlichen, welches von Descroizilles zuerst zu Grunde gelegt worden ist. Die
alkalimetrischen Methoden Gay-Lussac's und anderer
Chemiker sind nur Modificationen der ursprünglichen Prüfungsweise, welche theils zum
Zwek haben, die Ausführung der Operation zu erleichern, theils die Sicherheit der
Resultate zu steigern. Diese Methoden sind im Leben schon so eingebürgert, sie sind
selbst dem Fabrikanten so geläufig, daß wir hier eine nähere Beleuchtung des zu
Grunde liegenden Princips füglich übergehen können.
Die Bedingungen zur erfolgreichen Ausführung der auf das Descroizilles'sche Princip gegründeten Methoden lassen sich leicht durch genaue Arbeit,
durch richtige Apparate, durch Uebung und Geduld erfüllen, sofern der zu prüfenden
Potasche oder Soda nicht Salze oder Verunreinigungen beigemengt sind, welche die
Schwefelsäure in gleicher Weise abstumpfen, wie die kohlensauren Alkalien. Salze
dieser Art sind sowohl in den Pflanzenaschen, als ganz be sonders in der künstlichen
Soda, jederzeit bald in kleinerer, bald in größerer Menge vorhanden und zwar in den
ersteren insbesondere kieselsaures und phosphorsaures Alkali, kohlensaure,
phosphorsaure und kieselsaure alkalische Erden, in der lezteren schwefligsaures und
unterschwefligsaures Natron, Schwefelnatrium und in der rohen Soda außerdem
kohlensaurer Kalk und Schwefelcalcium. Von diesen Salzen können die in Wasser
unlöslichen (die Erdsalze) durch Behandeln der Probe mit Wasser und Filtriren
abgeschieden werden. Die Entfernung der löslichen aber ist entweder sehr umständlich
(Sodasorten, welche schwefligsaure Salze oder alkalische Schwefelmetalle enthalten,
müssen, ehe sie geprüft werden können, mit chlorsaurem Kali geschmolzen werden) oder
aber, was Verunreinigung mit unterschwefligsauren, kieselsauren oder phosphorsauren
Salzen betrifft, geradezu unmöglich. Die Anwesenheit dieser Salze ist die Ursache,
daß die Gehaltprüfungen der Potaschen- und Sodasorten nach den bisherigen
Methoden auf völlige Richtigkeit nicht Anspruch machen können, sobald die Menge der
fraglichen Verunreinigungen irgend bemerklich ist; sie ist die Veranlassung, daß der
Procentgehalt der Potasche und Soda an kohlensauren Alkalien fast immer zum
Nachtheile des Käufers zu hoch ausfällt — ein Fehler, dem sich fast alle
übrigen, die über haupt bei der Bestimmung gemacht werden können, hinzuaddiren.
— Wie erheblich und bedeutend dieser Einwurf sey, erhellt am deutlichsten
daraus, daß beinahe sämmtliche im Handel vorkommende Sodasorten so bemerkbare Mengen
von schwefligsaurem oder unterschwefligsaurem Natron enthalten, daß man nach den
bisherigen Methoden bei vielen Sorten kaum annähernde Resultate (3, 4, 6 und mehr
Proc. zu viel) erhalten kann — ein Umstand, welcher dadurch an Bedeutung
gewinnt, daß der Verbrauch der Potasche und der aus Pflanzenasche dargestellten Soda
gegen den der künstlichen Soda kaum mehr in Betracht kommt.
Faßt man das Gesagte kurz zusammen, so ergibt sich, daß die bisher üblichen
alkalimetrischen Methoden bei Abwesenheit von Schwefelmetallen und kieselsauren,
phosphorsauren, schwefligsauren und unterschwefligsauren Salzen gute Resultate
liefern werden, im Falle der Arbeitende Uebung hat und die anderweitigen Bedingungen
genau erfüllt sind, daß aber bei Anwesenheit der genannten Salze, von denen die
Potasche- und Sodasorten, wie erwähnt, fast nie frei sind, die Erlangung genügender
Resultate entweder mit bedeutenden Umständen verknüpft oder aber unmöglich ist.
Wenn man in Erwägung zieht, welche Chemiker sich schon mit der Verbesserung der auf
das bisher angewendete Princip gestüzten Methoden beschäftigt haben und die im
höchsten Grade sinnreichen Abänderungen, welche mit der Zeit in Vorschlag gekommen
sind, ins Auge faßt, so gelangt man zu der Ueberzeugung, daß die besprochenen Fehler
nicht Folge mangelhafter Angaben in Bezug auf die Ausführung der Operation sind,
sondern daß sie aus dem zu Grunde gelegten Princip unmittelbar hervorgehen und nicht
umgangen werden können, so lange dieses beibehalten wird.
Die Prüfungsmethode, deren wir uns bedienen und welche im Folgenden nunmehr
besprochen werden soll, beruht auf einem andern, auf einem nicht minder
naheliegenden und einfachen, dem früheren aber geradezu entgegengesezten
Princip.
Wenn man die Menge eines zusammengesezten Körpers finden will, dessen Bestandtheile
in einem bekannten, bestimmten und unveränderlichen Verhältnisse stehen, so ist es
nicht nothwendig, die Menge aller Bestandtheile zu bestimmen, die Kenntniß der
Quantität des einen oder des andern reicht schon hin, die Menge des Ganzen zu
ermitteln. — Der Zwek der Potasche- und Sodaprüfung ist die Bestimmung
des kohlensauren Alkali's in denselben. Nach dem eben angeführten Saze kann dieselbe
(angenommen die Kohlensäure und die Alkalien stünden in bestimmten Verhältnissen)
sowohl aus der Menge des Alkali's, als aus der der Kohlensäure gefunden werden. Die
bisherige Methode der Alkalimetrie nun suchte ihren Zwek zu erreichen, indem sie die
Menge des Alkali's bestimmte, und zwar durch Abmessen der
Säure, welche zu seiner Neutralisation erfordert wurde, nach der unseren gelangt man
zum Ziele, indem man die Menge der Kohlensäure bestimmt,
welche mit den Alkalien verbunden war.
Um auf dieses Princip eine Methode der Prüfung zu gründen, war die erste und
wesentlichste Bedingung, eine Bestimmungsweise der Kohlensäure zu ermitteln, welche
den Ansprüchen der Technik in jeder Hinsicht genügte.
Zur Bestimmung der Kohlensäure wendet man, wie bekannt, Verschiedene Methoden an.
Entweder glüht man die zu analysirenden Verbindungen für sich, oder unter Zusaz
solcher Substanzen, welche die Kohlensäure von ihren Basen abscheiden und findet
ihre Menge durch den Gewichtsverlust; bei weitem häufiger aber bestimmt man sie auf
nassem Wege und zwar entweder, indem man sie in eine Flüssigkeit (Kalilauge) leitet,
von welcher sie verschlukt wird, wobei sich also ihre Menge aus der Gewichtszunahme ergibt, oder
indem man sie durch Zusaz überschüssiger Säure mit der Vorsicht austreibt, daß
gleichzeitig keine anderen Materien, namentlich kein Wasser, verloren gehen, wobei
ihre Quantität aus der Gewichtsabnahme gefunden wird. Von diesen sämmtlichen
Methoden konnte sich, wie man auf den ersten Blik ersieht, zu technischen Zweken nur
die leztere eignen, zu deren Ausführung bereits die mannichfaltigsten Apparate von
Berzelius, H. Rose, Fritzsche,
Erdmann und Marchand und andern beschrieben
worden sind. Wir bedienten uns früher zu diesem Zwek eines höchst einfach
construirten Apparates, der sehr geeignet ist, den Vorgang möglichst zu
versinnlichen.
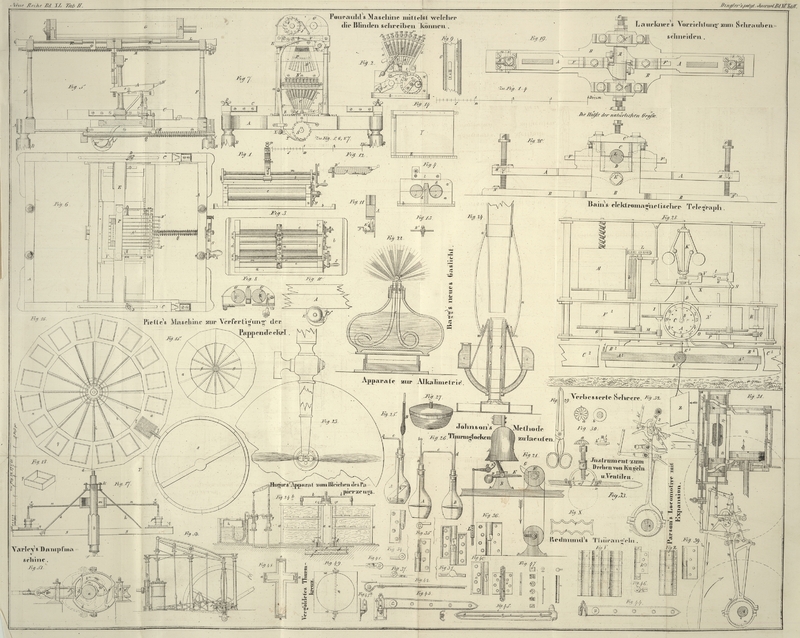
Man bringt in ein kleines Sezkölbchen A, Fig. 25, die zu
analysirende kohlensaure Verbindung in dem Röhrchen a,
die Säure, welche zur Zersezung dienen soll (Salzsäure, oder besser verdünnte
Schwefelsäure) in das Röhrchen b, welches so lang seyn
muß, daß es sich nicht waagrecht legen kann, verschließt alsdann das Kölbchen mit
einem Korke, in welchen erstlich eine Röhre mit Chlorcalcium, B, gepaßt ist und durch den ferner eine dünne Glasröhre c geht, welche mit ihrem einen Ende bis fast auf den
Grund von A reicht, an ihrem äußeren Ende aber durch ein
Wachskügelchen d verschlossen wird. Der so zugerichtete
Apparat wird gewogen und die Säure alsdann durch Neigen des Kölbchens allmählich aus
dem Röhrchen b ausgegossen. Die Kohlensäure wird
hierdurch ausgetrieben, sie entweicht durch die Chlorcalciumröhre und läßt ihre
Feuchtigkeit in derselben zurük. Nach beendigter Entwiklung, welche man zulezt durch
Wärme unterstüzt, wird die noch im Apparat befindliche Kohlensaͤure
verdrängt, indem man das Wachskügelchen wegnimmt, an die Röhre c mittelst eines Kautschukröhrchens ein Chlorcalciumrohr
befestigt, und an B saugt, bis die leztkommende Luft
nicht mehr nach Kohlensäure schmekt. Der Apparat wird nunmehr wieder gewogen; der
Gewichtsverlust gibt die Menge der Kohlensäure an, welche in der Verbindung
enthalten gewesen ist.
Dieser Apparat gibt sehr genaue Resultate; er läßt dem Chemiker kaum etwas zu
wünschen übrig. Unserem Zweke konnte er jedoch nicht genügen, indem damit nur so
kleine Mengen von Substanz zersezt werden können, daß eine höchst empfindliche Waage
erfordert wird, wenn man genaue Resultate erhalten will. Wir construirten daher
einen neuen Apparat, bei welchem das Austroknen der Kohlensäure nicht, wie bei den
sämmtlichen früheren Apparaten durch Chlorcalcium, sondern auf die einfachste Weise
durch dieselbe Schwefelsäure bewirkt wird, mittelst welcher man die Kohlensäure aus
ihren Verbindungen austreibt. Derselbe gestattet eine Zersezung sehr beträchtlicher Mengen
Substanz; man ist bei seinem Gebrauche nie in Sorge, zu wenig Säure zu haben. Die
Zurükhaltung des Wassers geschieht bei weitem vollständiger, als es durch
Chlorcalcium bei einigermaßen rascher Gasentwikelung möglich ist. Das Zuführen von
Wärme wird unnöthig, indem die Schwefelsäure diesen Dienst ebenfalls versieht
— die Genauigkeit und Constanz der Resultate auch bei Anwendung ganz
gewöhnlicher Apothekerhandwaagen mit Schnüren und Hornschalen, die Leichtigkeit, mit
welcher genaue Resultate von jedem erhalten wurden, überstieg weit unsere Erwartung;
die Einfachheit des Apparates endlich macht es möglich, daß er von jedem überaus
leicht selbst verfertigt werden kann, wie aus dem Folgenden sogleich zu ersehen
ist.
A und B, Fig. 26, sind zwei
Kölbchen, welche auch durch Medicingläser ersezt werden können, wenn dieselben
hinlänglich weite Oeffnungen haben. A fasse etwa
4–5 Loth Wasser, B wählt man zwekmäßig etwas
kleiner, von 3–4 Loth Inhalt. Die Kölbchen werden mit Korkstopfen
verschlossen, deren jeder zweimal durchbohrt ist. Die Löcher nehmen die Glasröhren
b, c und d in der Weise
auf, wie es Fig.
26 zeigt. Die Enden aller Röhren sind offen; bei dem Gebrauche wird die
Röhre a an ihrem Ende b
durch ein Wachskügelchen verschlossen. In A schüttet man
die abgewogene Substanz und füllt alsdann das Kölbchen zu einem Drittheil mit Wasser
an, B wird mit gewöhnlicher englischer Schwefelsäure
halb voll gemacht. Die Stopfen werden alsdann eingedreht, und der Apparat gewogen.
Man saugt nunmehr aus der Röhre d etwas Luft aus, und
verdünnt somit die Luft im ganzen Apparate. Die Folge davon ist, daß die in B befindliche Schwefelsäure in der Röhre c in die Höhe steigt, und daß ein Theil derselben in das
Kölbchen A herüberfließt. Sowie sie aber in die Lösung
des kohlensauren Salzes kommt, beginnt sogleich eine lebhafte Entwikelung von
Kohlensäure. Zufolge der Einrichtung des Apparates muß dieselbe durch die
Schwefelsäure in B streichen, bevor sie aus der Röhre
d, der einzigen Oeffnung des Apparates, entweichen
kann, bei welchem Durchstreichen ihre Feuchtigkeit begreiflichermaßen vollständiger,
als auf jede andere Weise, aufgenommen und zurükgehalten wird. Bei dem Einfließen
der Schwefelsäure erwärmt sich die Flüssigkeit in A und
dehnt sich hierdurch nebst der darüber befindlichen Luft aus; beim Erkalten nehmen
beide ihr ursprüngliches Volumen wieder ein, was zur Folge hat, daß eine neue
Portion Schwefelsäure nach A herüberfließt, sobald die
Gasentwikelung aufgehört hat. Diese eine Ursache des sich von selbst wiederholenden
Herüberfließens der Schwefelsäure wird im Anfange der Operation noch durch eine
andere, nämlich dadurch unterstüzt, daß die in A befindliche
Kohlensäure von dem noch nicht zersezten kohlensauren Alkali absorbirt wird, indem
sich anderthalbfach oder doppelt kohlensaures Alkali bildet. Wollte man jedoch das
erneuerte Hinüberfließen der Schwefelsäure den genannten Ursachen allein überlassen,
so würde ein Versuch eine ziemlich lange Zeit in Anspruch nehmen; bei weitem
einfacher ist es daher, wenn man jedesmal nach beendigter Gasentwikelung die Luft im
Apparate wiederum ebenso wie im Anfange verdünnt, indem man aus der Röhre d etwas Luft aussaugt. Die Operation läßt sich auf diese
Weise in wenigen Minuten beendigen. Ist das kohlensaure Salz vollständig zersezt,
was man sogleich daraus ersieht, daß beim Hinzukommen neuer Säure keine
Gasentwikelung mehr erfolgt, so bewirkt man durch erneuertes Saugen, daß von der in
B noch befindlichen Schwefelsäure eine etwas größere
Menge nach A hinüberfließt. Hierdurch erwärmt sich die
Flüssigkeit so stark, daß alle Kohlensäure, welche sie absorbirt hatte, entweicht.
So wie nun die Gasentwikelung völlig aufgehört hat, öffnet man das Ende der Röhre
a, indem man das Wachskügelchen lüftet, und saugt
bei d so lange, bis alle Kohlensäure, mit welcher der
Apparat noch erfüllt war, durch Luft ersezt ist, bis man also bei weiterem Aussaugen
reine Luft bekommt. Den Apparat läßt man alsdann erkalten, troknet ihn ab und wägt
ihn. Der Gewichtsverlust gibt die Menge der Kohlensäure, welche in der Probe
enthalten war, mit größter Genauigkeit an. Auf wie einfache Weise man aus der
gefundenen Kohlensäuremenge den Gehalt der Potasche oder Soda an kohlensauren
Alkalien finden kann, werden wir in der Folge sehen.
Diese eben angeführte Bestimmungsweise der Kohlensäure ist die Grundlage der
sämmtlichen Prüfungsmethoden, welche wir nicht allein zur Alkalimetrie, sondern auch
zur Prüfung der Säuren und des Braunsteins anführen werden. Der beschriebene und
unter Fig. 26
dargestellte Apparat ist das Mittel zu ihrer Ausführung.
Bevor wir zur Beschreibung der Einzelnheiten der Methode übergehen, halten wir es für
nöthig, die Versuche anzuführen, durch welche wir uns von der Genauigkeit der
Resultate überzeugten, die mit unserem Apparate erhalten werden. Die Versuche
stellten wir in der Art an, daß wir erstens chemisch reines kohlensaures Natron, und
daß wir ferner gleichsam künstliche Sodasorten von völlig bekanntem Gehalt, durch
Zusammenmischen von kohlensaurem Natron mit Glaubersalz bereitet, untersuchten. Alle
Versuche wurden absichtlich mit gewöhnlichen Apothekerhandwaagen angestellt.
1.
4,83
reinen kohlensauren Natrons gaben Kohlensäure
2,010
2.
4,83
ddo. gaben Kohlensäure
1,995
3.
4,83
—
—
2,020
4.
2,56
—
—
1,062
5.
4,255
krystallisirten kohlens. Natrons gaben Kohlensäure
0,665
6.
4,275
ddo. gaben Kohlensäure
0,655
Es gab Kohlensaͤure:
Es haͤtte geben muͤssen:
1.
41,61
41,30
2.
41,30
—
3.
41,82
—
4.
41,45
—
5.
15,39
15,35
6.
15,55
—
Aus diesen Angaben ersieht man auf den ersten Blik daß die gefundenen Mengen mit den
berechneten eine selbst den strengsten Anforderungen genügende Uebereinstimmung
zeigen — eine Uebereinstimmung, wie sie nur bei den besten chemischen
Analysen getroffen wird. Man ersieht ferner aus den obigen und den weiter unten
mitgetheilten Versuchen, daß diese Bestimmungsweise der Kohlensäure keine
Fehlerquelle hat, welche ihre Menge constant zu groß oder zu gering finden ließe;
die gefundenen Zahlen sind bald etwas höher, bald etwas niederer als die
berechneten, woraus hervorgeht, daß die Differenzen lediglich Folge von nie zu
vermeidenden kleinen Beobachtungsfehlern bei der Gewichtsbestimmung der verwendeten
Substanz und des Apparates sind, welche mehr oder weniger mit dem
Feuchtigkeitszustande der Luft und der nicht völlig gleichen Temperatur des
Apparates vor und nach dem Austreiben der Kohlensäure zusammenhängen.
Es ist nun noch der Einfluß zu besprechen, den die der Potasche und Soda fast immer
beigemengten fremden Salze, wie Chlormetalle, Schwefelmetalle, schwefligsaure und
unterschwefligsaure Salze ausüben, wenn man den obigen Apparat zur Alkalimetrie, zur
Bestimmung des Handelswerthes der käuflichen Potasche und Soda anwenden will.
Vorhandene Chlormetalle veranlassen, wie wir uns durch Versuche überzeugt haben,
keinen Fehler, da bei dem Zustande der Verdünnung, in welchem die Lösung der Probe
sich befindet, von der freigewordenen Salzsäure keine Spur entweicht. Dem
schädlichen Einfluß, der durch die Gegenwart von Schwefelmetallen, schwefligsauren
und unterschwefligsauren Salzen auf das Resultat ausgeübt würde, beugt man sehr
leicht vor, indem man die Lösung der zu prüfenden Potasche oder Soda mit einer
kleinen Quantität neutralen chromsauren Kalis versezt. Sowohl die schweflige Säure
als der
Schwefelwasserstoff werden dadurch im Momente des Freiwerdens zersezt, unter Bildung
von schwefelsaurem Chromoxyd, Wasser und Schwefel, welche in der Lösung
zurükbleiben.
Die Fehlerquellen, welche von anderen in der Potasche und Soda vorhandenen Salzen
herrühren, lassen sich also überaus leicht beseitigen, es muß aber noch ein anderer
Umstand erwogen werden, ehe unsere Methode fehlerfrei dasteht. Es ist nämlich in
Frage zu stellen, ob sich aus der gefundenen Menge der Kohlensäure auch wirtlich
immer genau der Handelswerth der Potasche und Soda in dem oben festgestellten Sinne
ergibt. Diese Frage wird durch die Beantwortung einer andern, der folgenden,
entschieden. Steht in dem löslichen Theile der Potasche und Soda die Menge der
Kohlensäure zu der Menge des Alkalis, welches beim Behandeln ihrer Lösungen mit Kalk
kaustisch wird, welches also ihren Handelswerth im engeren Sinne bedingt, in einem
bestimmten und constanten, oder in einem unbestimmten und wechselnden
Verhältniß?
Ist die leztere Ansicht die richtige, so ist die neue Methode dem Princip nach
falsch; ist hingegen das Verhältniß ein bestimmtes und unveränderliches, oder kann
dieses Verhältniß, falls es noch nicht besteht, auf einfache Art hergestellt werden,
so sind alle und jede Einwürfe widerlegt, welche unserer Bestimmungsweise gemacht
werden können.
Nach der allgemein angenommenen Ansicht ist das fragliche Verhältniß ein bestimmtes.
Wer ist damit nicht einverstanden, daß Potasche und Soda neutrales kohlensaures Kali
enthalten! In der neueren Zeit jedoch sind Abweichungen von diesem bestimmten
Verhältnisse und zwar nach zwei entgegengesezten Seiten hin angegeben worden. Nach
den einen Angaben soll in der Potasche und Soda die Kohlensäure zuweilen in
geringerem Verhältnisse zum Alkali stehen, als im neutralen kohlensauren Kali oder
Natron, nach anderen in höherem. Nach den ersten findet sich in manchen
Potasche- und Sodasorten kaustisches Alkali neben neutralem kohlensaurem,
nach den lezteren zweifach, anderthalbfach und nach einer sogar neun Achtel
kohlensaures Alkali. — Unsere Aufgabe ist es, die Richtigkeit dieser Angaben
an und für sich zu prüfen, die Umstände, von denen die besprochenen Abweichungen
abhängen, zu beleuchten; die Zeichen, welche solche anomale Potasche- und
Sodasorten erkennen lassen, zu ermitteln, so wie auseinanderzusezen, ob diese
Anomalien auf die Richtigkeit unserer alkalimetrischen Prüfungsweise einen
nachtheiligen Einfluß von Belang haben und auf welche Art derselbe aufgehoben werden
kann. Zuvor aber machen wir noch darauf aufmerksam, daß unserer Methode eine
Fehlerquelle jedenfalls bleibt, nämlich die, daß kohlensaures Natron, falls es
in der Potasche vorhanden ist, als kohlensaures Kali in Rechnung kommt und vice versa. Handelt es sich jedoch bloß um bestimmte
Aequivalente Alkali, die man, gleichsam nur als Träger einer Kraft, als Mittel zur
Erzeugung einer bestimmten chemischen Wirkung benüzen will, so bekommt man
vollkommen das richtige Resultat, denn um so viel kleiner die Aequivalentzahl des
Natrons ist, als die des Kalis, um so viel mehr Kali wird ja statt des Natrons in
Rechnung gebracht. Oder mit andern Worten ausgedrükt, kann man sagen, die
Kohlensäure ist proportional der Kraft und Wirkung, sowohl der Potasche, als der
Soda oder eines Gemenges von beiden; überträgt man die aus einer bestimmten Menge
entwikelte nach Aequivalenten auf irgend eine beliebige andere Säure, so wird eine
gleiche Menge des kohlensauren Alkalis von der gefundenen Säurequantität genau
neutralisirt. — Kommt aber das kohlensaure Kali als solches, als Kali-Salz, in Betracht, so gibt die Kohlensäure
natürlicherweise über das Mengenverhältniß desselben keinen Aufschluß.
Dieser Uebelstand ist jedoch nicht unserer Methode eigenthümlich, sondern er kommt
allen bekannten alkalimetrischen Methoden in völlig gleichem Maaße zu.
Was das kaustische Kali betrifft, so kommt dasselbe
unläugbar in nordamerikanischen Potaschen vor. Es verdankt seinen Ursprung dem
Umstande, daß bei der Bereitung gebrannter Kalk zugesezt wurde; seine Menge ist
abhängig von der Menge des zugefügten Kalkes. Nach einigen Angaben soll auch bei der
Calcination der rohen Potasche Aezkali gebildet werden durch Einwirkung von Kohle,
überhaupt organischer Materie, auf das kohlensaure Alkali. Wir wollen lezterer
Ansicht nicht geradezu widersprechen, indem wir nicht läugnen, daß auf diese Weise
äzendes Kali gebildet werden könne; sie scheint aber einigermaßen unwahrscheinlich,
weil sich bei der Temperatur, bei welcher die Zersezung erst vor sich gehen kann,
jedenfalls auch Schwefelkalium bilden müßte, was bei den deutschen, illyrischen etc.
Potaschen bekanntlich nicht der Fall ist, und weil ferner bei der Calcination, wie
sie jezt geschieht, die Masse im Flammfeuer, also in einer an Kohlensäure reichen
Atmosphäre erhizt wird, in welcher sich gebildetes Aezkali sogleich wieder mit
Kohlensäure sättigen würde. Als Thatsache können wir anführen, daß die sämmtlichen
Sorten Potasche, welche wir im Handel fanden (illyrische, böhmische, deutsche u. s.
w.), keine Spur äzendes Alkali enthielten, wovon wir uns nicht allein nach der
weiter unten beschriebenen Methode, sondern auch noch dadurch überzeugten, daß wir
geglühte Proben wogen, mit einer concentrirten Lösung von kohlensaurem Ammoniak
befeuchteten, und nach
dem Verdampfen der Flüssigkeit wiederum glühten und wogen. Keine Probe nahm
hierdurch an Gewicht zu. Kaustisches Kali hat man also nur in sehr seltenen Fällen,
in der Regel nur bei gewissen nordamerikanischen Potaschen zu fürchten.
Was das kaustische Natron betrifft, so findet sich
dasselbe ziemlich häufig in den im Handel vorkommenden Sodasorten. Es verdankt
seinen Ursprung der Umsezung des kohlensauren Natrons mit dem bei der Calcination
kaustisch gewordenen kohlensauren Kalk und findet sich allezeit in der Soda, wenn
dieselbe nicht durch Krystallisation von dem Schwefelcalcium getrennt worden ist,
oder wenn die Lauge nicht so lange der Luft ausgesezt war, daß sie sich wiederum
vollständig mit Kohlensäure sättigen konnte.
Doppelt-, richtiger anderthalbkohlensaures Kali oder Natron bildet
sich in der Potasche und Soda durch Aufnahme von Kohlensäure aus der atmosphärischen
Luft, wenn dieselben längere Zeit mit der Luft in Berührung sind. Seine Menge ist
nach unseren Versuchen in der Regel höchst gering, in den meisten Fällen kaum
entdekbar. Um es nachzuweisen, versezt man die Lösung der zu prüfenden Potasche oder
Soda mit Chlorcalciumlösung im Ueberschuß, filtrirt und sezt zum Filtrat Ammoniak.
Eine sogleich entstehende Trübung gibt es zu erkennen. Gleichgültig übrigens, ob es
vorhanden ist oder nicht, es geht beim gelinden Glühen in neutrales kohlensaures
Salz über und ist somit, da nach unserer Methode ein Erhizen der Probe nie umgangen
werden kann, auf das Resultat ohne Einfluß.
Diese Angabe aller Chemiker, daß nämlich anderthalb oder doppelt kohlensaures Kali
beim Glühen in neutrales Salz übergehe, ist kürzlich von Hermann (Journal für praktische Chemie, Bd. XXII S. 442) in Abrede gestellt worden. Derselbe gibt an, daß der Rükstand
nicht neutrales, sondern neunachtel kohlensaures Alkali sey, und stüzt seine Angabe
auf zwei Analysen: eine vom Rükstand des kohlensauren Kalis, die andere von dem des
kohlensauren Natrons. Derselbe gibt ferner an, daß auch in der Potasche kein
neutrales, sondern ebenfalls neunachtel kohlensaures Kali enthalten sey. Diese
Angaben klingen so unwahrscheinlich, daß wir zu unserer eigenen Ueberzeugung kaum
der Versuche bedurft hätten, um von ihrer Unrichtigkeit überzeugt zu seyn. Da aber
Zahlenresultate nur wiederum durch Zahlen widerlegt werden können, und da es von
größter Wichtigkeit ist, daß sich unrichtige Angaben der Art nicht in die
Wissenschaft einschleichen, so sahen wir uns genöthigt, die Hermann'schen Untersuchungen zu wiederholen. Die folgenden Resultate
unserer Analysen mögen über ihre Richtigkeit entscheiden.
a) Untersuchung des
Ruͤkstandes, der beim Gluͤhen von chemisch reinem doppeltkohlensaurem
Kali blieb.
1. 2,8135 Gram. gaben mit unserem Apparate 0,855 Kohlensäure.
2. 3,4488 Gram. gaben 1,0985 Kohlensäure, dieß entspricht in 100 Theilen
I.
II.
berechnet als neutrales Salz.
Kohlensäure
31,45
—
31,85
—
31,80
Kali
68,55
—
68,15
—
68,20
–––––––––––––––––––––––––––––––––––––––––––––
100,00
—
100,00
—
100,00
Neunachtelkohlensaures Kali würde verlangen
Kohlensäure
34,47
Kali
65,63
––––––––
100,00.
b) Untersuchung des
Ruͤkstandes, der beim Gluͤhen von chemisch reinem doppeltkohlensaurem
Natron blieb:
1.
2,498
Gram.
gaben
1,0247
Kohlensäure
2.
2,7881
—
—
1,1565
—
dieß entspricht in 100 Theilen
I.
II.
berechnet als neutrales Salz.
Kohlensäure
41,02
—
41,48
—
41,29
Natron
58,98
—
58,52
—
58,71
–––––––––––––––––––––––––––––––––––––––––––––
100,00
—
100,00
—
100,00.
Neunachtel kohlensaures Natron würde verlangen
Kohlensäure
44,18
Natron
55,82
–––––––
100,00.
Diese Zahlen beseitigen jeden Zweifel über die chemische Constitution der bleibenden
Rükstände; sie zeigen evident, daß eben so wenig ein neunachtel kohlensaures Alkali,
als überhaupt eine Verbindung, welche mehr Kohlensäure enthält als den neutralen
Salzen entspricht, bei höherer Temperatur bestehen kann, und geben somit den
Schlußstein zu dem von uns zu führenden Beweise in vollgültiger Weise ab.
Specielle Anleitung zur praktischen
Ausführung der Potasche- und Sodaprüfung.
Um den Handelswerth der Potasche und Soda genau beurtheilen zu können, muß man ihren
Wassergehalt und die Menge des kohlensauren Alkalis kennen. Der Gang der Untersuchung, welcher diese
Kenntniß verschafft, bleibt sich nicht unter allen Umständen gleich; er ist abhängig von der
Abwesenheit oder Gegenwart gewisser chemischer Verbindungen, welche größtentheils
als Verunreinigungen der Potasche und Soda zu betrachten sind. Die Beimengungen,
welche eine Modification des Verfahrens bedingen, sind äzende, schwefligsaure und
unterschwefligsaure Alkalien, Schwefelmetalle und kohlensaure Erden. Man erkennt
ihre Gegenwart und beseitigt ihren schädlichen Einfluß auf das Resultat der Prüfung
leicht auf folgende Weise:
1) Kohlensaure alkalische Erden. — Man übergießt
eine Probe der zerriebenen Potasche oder Soda mit heißem Regenwasser. Löst sie sich
klar auf oder bleiben nur wenige Floken ungelöst, so kann man von der Abwesenheit
kohlensaurer Erden überzeugt seyn. Bleibt hingegen ein weißes Pulver zurük, welches
nach dem Auswaschen mit Säuren braust, so ist die Gegenwart von kohlensaurem Kalk
oder kohlensaurer Magnesia erwiesen. In diesem Falle muß die abgewogene Probe mit
heißem Regenwasser übergossen, die Lösung abfiltrirt, der Rükstand ausgewaschen und
das Filtrat, welches nöthigenfalls etwas abgedampft wird, in das Kölbchen A gebracht werden.
2) Schwefligsaure und unterschwefligsaure Salze. —
Sie kommen nur in der Soda, nie in der Potasche vor. Man überzeugt sich am
schnellsten und sichersten von ihrer Anwesenheit, indem man etwa 2 Loth verdünnter
Schwefelsäure mit etwas chromsaurem Kali rothgelb färbt und zu derselben alsdann von
der zu prüfenden Soda hinzufügt, jedoch so daß die Flüssigkeit immer noch sauer
bleibt. Geht die rothgelbe Farbe in eine grüne über, so waren die genannten Salze
vorhanden. Schwefelnatrium veranlaßt zwar dieselbe Farbenveränderung; so oft sich
aber dieses findet, kann man sicher annehmen, daß auch unterschwefligsaures Natron
zugegen ist. Die alkalischen Schwefelmetalle findet man
am leichtesten, indem man die fragliche Potasche oder Soda mit einer Lösung von
gewöhnlichem (anderthalb-) kohlensaurem Ammoniak befeuchtet. Im Falle sie
zugegen sind, entwikelt sich sogleich Schwefelammonium, welches leicht an seinem
Geruch und an der Eigenschaft erkannt werden kann, ein mit Bleizukerlösung
befeuchtetes Papier zu schwärzen. — Wenn eine oder die andere dieser
Beimengungen vorhanden ist, so sezt man bei der Kohlensäurebestimmung eine
Messerspize voll neutralen chromsauren Kalis zu.
3) Aezkali und Aeznatron. — Man übergießt 1 Theil
der zu prüfenden Potasche oder Soda nebst etwa 3 Theilen Chlorbaryums mit heißem
Wasser, rührt um und prüft die Flüssigkeit, nachdem man etwas davon abfiltrirt hat,
mit Georginen- oder Curcumapapier. Wird ersteres grün oder lezteres braun, so
ist Aezkali zugegen. Es versteht sich von selbst, daß das Chlorbaryum völlig neutral
und ferner, daß es im Ueberschuß vorhanden seyn muß, wovon man sich im Zweifelsfalle
leicht überzeugt, wenn man zum Filtrat nochmals etwas Chlorbaryum zusezt, wodurch
kein Niederschlag mehr entstehen darf. Diese Prüfungsweise verdient ihrer
Einfachheit und Sicherheit wegen den übrigen zu gleichem Zweke vorgeschlagenen
unstreitig vorgezogen zu werden. Sollte Schwefelkalium oder Schwefelnatrium, die
ebenfalls eine alkalische Reaction veranlassen würden, vorhanden seyn, so braucht
man auf äzende Alkalien nicht weiter zu prüfen; man kann sicher seyn, daß sie sich
alsdann jederzeit vorfinden.
Im Falle äzende Alkalien vorhanden sind, zerreibt man die zur Kohlensäurebestimmung
abgewogene Probe mit 3–4 Theilen reinen Quarzsandes, mengt
¼–⅓ von der Menge der Probe gepulverten kohlensauren Ammoniaks
zu, bringt das Pulver in ein Schälchen, spült die Reibschale, im Falle etwas hängen
geblieben ist, mit etwas Sand nach, tröpfelt so viel Wasser auf die Masse, als sie
einsaugen kann, läßt sie eine kleine Weile stehen und erhizt alsdann bis alles
Wasser und kohlensaure Ammoniak ausgetrieben ist. Enthält eine Potasche oder Soda
neben dem äzenden Alkali noch alkalisches Schwefelmetall, so nimmt man statt des
Wassers zum Befeuchten der Masse Salmiakgeist, um das anderthalb kohlensaure
Ammoniak in neutrales zurükzuführen; andernfalls würde Schwefelammonium entwikelt
und ein Theil des alkalischen Schwefelmetalls in kohlensaures Alkali übergeführt
werden. Nach dem Erkalten bringt man die Masse, welche sich mit Hülfe eines Messers
auf die leichteste Art aus dem Schälchen nehmen läßt, in den Kolben A, spült das Schälchen mit etwas Wasser nach und
verfährt genau wie unten beschrieben wird. Der Sand dient dazu, das Zusammenbaken
der Masse, so wie das Sprizen beim Eintroknen zu verhüten.
Zur Bestimmung des Wassergehaltes der Potasche und Soda
bringt man ein Schälchen von Eisenblech, welches etwa 2 Zoll Durchmesser hat und mit
einem etwas lose schließenden Dekel versehen ist (Fig. 27), oder einen
Porzellantiegel sammt seinem Dekel auf die eine Schale einer gewöhnlichen, aber
genauen Handwaage, beschwert dieselbe Schale mit einem Zehngrammstük und bringt die
Waage durch Schrote, zulezt durch Staniolstreifen genau ins Gleichgewicht. Man nimmt
nun von der zu untersuchenden Potasche oder Soda an verschiedenen Stellen Proben
heraus, zerreibt sie, entfernt alsdann das Zehngrammstük von der Waage und bringt
statt dessen so lange von dem Pulver in das Schälchen, bis das Gleichgewicht wieder völlig
hergestellt ist. Man hat auf diese Art genau 10 Gram. Potasche oder Soda in dem
Schälchen.
Dasselbe wird jezt über einer guten Weingeistlampe erhizt bis alles Wasser
ausgetrieben ist und nach dem Erkalten auf die Waage gebracht, auf welcher sich die
ursprüngliche Tara noch befindet. Die Anzahl der Decigramme, welche hinzugelegt
werden müssen, um das Gleichgewicht herzustellen, gibt alsdann den Wassergehalt in
Procenten an.
Von der auf diese Art erhaltenen wasserfreien Potasche wiegt man 6,29 Gram., von der
wasserfreien Soda aber 4,84 Gram. ab, bringt die Probe mittelst eines Kartenblattes
in das Kölbchen A des Apparates Fig. 26, welches man
alsdann zu etwa ⅓ mit Wasser füllt.Bei Sodasorten wird in den oben erwaͤhnten Faͤllen dem Wasser
noch etwas neutrales chromsaures Kali zugesezt, oder man nimmt geradezu eine
mit Ammoniak etwas uͤbersaͤttigte Loͤsung von saurem
chromsaurem Kali. Man tarirt nun den abgetrokneten und wie oben
angegeben zugerüsteten Apparat, und bewirkt durch gelindes Saugen bei d, daß die Schwefelsäure aus dem Kolben B nach A hinübersteigt.Die ersten Tropfen der mit dem kohlensauren Alkali zusammenkommenden
concentrirten Schwefelsaͤure bringen eine heftige, stoßweise
Gasentwiklung hervor; man darf sich hiedurch nicht abhalten lassen, den
Versuch zu beendigen, da dieß auf das Resultat ohne den geringsten Einfluß
ist. Nach vollendeter Zersezung lüpft man das Wachskügelchen b etwas, saugt Luft durch den Apparat (wobei man sich
einer mit feuchtem Kalkhydrat gefüllten Röhre bedienen kann, wenn man den Geschmak
der Kohlensäure belästigend findet) bis alle Kohlensäure entfernt ist, bringt ihn
nach dem völligen Erkalten, das man durch Eintauchen des warmen Kölbchens in kaltes
Wasser beschleunigen kann, auf die Waagschale, und ersezt die entwichene Kohlensäure
durch Gewichte.
Die Zahl der Centigramme, welche zu dem Apparat gelegt werden mußten, um das
Gleichgewicht wieder herzustellen, dividirt durch 2, gibt unmittelbar die Procente
an wasserfreiem kohlensaurem Kali oder Natron an. Gesezt also, 6,29 Gram. Potasche
hätten gegeben 1,60 Gram. Gewichtsverlust des Apparates, oder was dasselbe ist,
Kohlensäure, so enthielte sie 160/2 = 80 Proc. kohlensaures Kali.
Die Bestimmung der Quantitäten von äzendem Natron oder Kali, welche neben den
kohlensauren Alkalien in der Potasche oder Soda enthalten seyn können, hat nicht
sowohl für den Handel, als für die Fabrication, namentlich aber für die Wissenschaft
Bedeutung. Zu ihrer Ausführung bietet unsere gewöhnliche alkalimetrische Methode das
einfachste Mittel dar.
Man wägt, je nachdem man mit Potasche oder Soda zu thun hat, 6,29 oder 4,84 Gram. des
entwässerten Rükstandes zweimal ab, bestimmt in der einen Portion die Kohlensäure
geradezu, in der anderen nach vorhergegangener Behandlung mit kohlensaurem Ammoniak.
Aus der Differenz der erhaltenen Gewichte findet man das Quantum des Aezkalis in
Procenten, indem man sie mit 34,101 multiplicirt; bei Soda muß sie mit 29,38
multiplicirt werden, um den Procentgehalt an Aeznatron zu finden.
Als Belege der Sicherheit der nach unserer Methode zu erhaltenden Resultate, als
Bürgschaft für ihre allgemeine Anwendbarkeit, als Anhaltspunkte zur Vergleichung
derselben mit der Gay-Lussac'schen
Verfahrungsweise und endlich als Beitrag zur Kenntniß des Gehalts der gegenwärtig in
hiesigen Gegenden zumeist verwendet werdenden Potasche- und Sodasorten,
theilen wir schließlich die Ergebnisse einiger von uns ausgeführter
Gehaltsbestimmungen mit.
Wir wendeten erstens, um bestimmte Controlen für die nach den verschiedenen
Prüfungsweisen erhaltenen Ergebnisse zu haben, künstlich gemengte Sodasorten, deren
Gehalt uns aufs Genaueste bekannt war, und zweitens im Handel vorkommende
Potasche- und Sodasorten an.
A. Analysen von Sodasorten, deren Gehalt genau bekannt war.
1) a. 4,84 Gram. eines Gemenges von gleichen Theilen
wasserfreien kohlensauren Natrons und wasserfreien Glaubersalzes gaben 1,002
Gram. Kohlensäure.
b. 3,185 desselben Gemenges sättigten 57,5°
Gay-Lussac'sche Probesäure.Die Schwefelsaͤure, deren wir uns als Probesaͤure
bedienten, war durch Faͤllung mit Baryt auf das Genaueste
titrirt.
c. 3,185 sättigten bei einem zweiten Versuche
58,4°.
2) a. 4,84 Gram. eines Gemenges von 2 Theilen
kohlensauren Natrons und 1 Theil Glaubersalz gaben 1,33 Gram. Kohlensäure.
b.
3,185
sättigten
80°
Probesäure.
c.
—
—
79,5°
—
d.
—
—
79°
—
3) 9,68 Gram. eines Gemenges von 1 Theil kohlensaurem Natron mit 3 Theilen
Glaubersalz gaben 0,997 Kohlensäure.
4) a. 4,84 reine kryst. Soda gaben 0,745
Kohlensäure.
b. 4,84 reine kryst. Soda gaben
0,753 Kohlensäure.
c. 3,185 sättigten 46°
Probesäure.
d. 3,185 sättigten 45°
Probesäure.
In 100 Theilen der analysirten Verbindungen sind demnach enthalten an
wasserfreiem kohlensaurem Natron:
Nach
unserer Meth.
Nach Gay-Lussac's Verfahren.
Berechnet.
1)
50,1
—
48,9
—
49,7
—
50,0
2)
66,5
—
68,1
—
67,7
—
67,3
—
66,6
3)
24,9
—
—
—
25,0
4)
37,2 — 37,6
—
39,1
—
38,2
—
37,2.
B) Analysen käuflicher Potaschesorten.
Die nachfolgenden Potaschesorten waren sämmtlich frei von Aezkali, Schwefelkalium
und kohlensaurem Kalk.
1) Böhmische Potasche. — 10 Gram. verloren
durch Erhizen 0,916 Gram.
6,29
Gram. gaben
1,893
Kohlensäure.
4,807
Gram. sättigten
131°
Probesäure.
2) Illyrische Potasche, erste Sorte. — 10 Gram.
Verloren 0,708 Gram. Wasser.
6,29 Gram. gaben
1,918 Gram. Kohlensäure.
4,807 Gram. sättigten
131,3° Probesäure.
3) Illyrische Potasche, zweite Sorte. — 10
Gram. verloren 1,24 Gram. Wasser.
6,29 Gram. gaben
1,875 Gram. Kohlensäure.
4,807 Gram. sättigten
131,3° Probesäure.
4) Sächsische Potasche. — 10 Gram. verloren
beim Erhizen 0,85 Gram.
6,29 Gram. gaben 1,225 Gram. Kohlensäure.
5) Heidelberger Potasche von Fries. — 10 Gram.
verloren beim Erhizen 0,112 Gram.
6,29
Gram. gaben Kohlensäure 1,36 Gram.
4,807
Gram. sättigten 111,2° Probesäure.
In den wasserfreien Potaschen sind demnach folgende Mengen kohlensauren Kalis in
Procenten ausgedrükt:
Nach unserer Methode.
Nach Gay-Lussac's Methode.
1)
94,6
—
96,0
2)
95,9
—
96,1
3)
93,8
—
96,1
4)
61,2
—
—
5)
68,0
—
68,9.
C. Analysen käuflicher Sodasorten.Die qualitativen Pruͤfungen sind nach den oben beschriebenen
Methoden ausgefuͤhrt.
1) Gelbe calcinirte niederländische Soda. — Die
selbe löste sich in Wasser ziemlich vollständig; der gelbliche, flokige Rükstand
war frei von kohlensaurem Kalk. Sie enthielt wenig kaustisches, viel
schwefligsaures und unterschwefligsaures Natron, kein Schwefelnatrium.
10 Gram. verloren beim Erhizen 1,97 Gram.
4,84 Gram. des Rükstandes gaben nach vorhergegangener Behandlung mit kohlensaurem
Ammoniak 1,670 Kohlensäure.
3,185 Gram. sättigten Probesäure 100,8°.
2) Weiße calcinirte niederländische Soda. —
Dieselbe ließ beim Behandeln mit Wasser einen flokigen, von kohlensaurem Kalk
freien Niederschlag zurük. Sie war frei von Aeznatron, von Schwefelnatrium, von
schwefligsaurem und unterschwefligsaurem Natron.
10 Gram. verloren beim Glühen 0,404 Gram.
4,84 Gram. des geglühten Rükstandes gaben Kohlensäure 0,876 Gram.
3,185 Gram. des geglühten Rükstandes sättigten Gay-Lussac'sche Probesäure 54,1°;–3,185 sättigten
bei einem zweiten Versuche 53,4°.
3. Dieusé-Soda. — Dieselbe war sehr
schön weiß, in Wasser fast vollständig löslich. Sie enthielt ziemlich viel
kaustisches Natron, kein schwefligsaures und unterschwefligsaures Natron, kein
Schwefelnatrium.
10 Gram. verloren beim Glühen 0,39.
4,84 Gram. des geglühten Rükstandes gaben nach vorhergegangener Behandlung mit
kohlensaurem Ammoniak 1,62 Gram. Kohlensäure.
3,185 Gram. des geglühten Rükstandes sättigten Gay-Lussac'sche Probesäure 93,l.
4) Casseler Soda. — Dieselbe war schön weiß,
ließ beim Behandeln mit Wasser einen reichlichen weißen, flokigen, von
kohlensaurem Kalk freien Rükstand, enthielt Aeznatron, schwefligsaures und
unterschwefligsaures Natron, kein Schwefelnatrium.
4,84 Gram. geglühter Soda gaben nach vorhergegangener Behandlung mit kohlensaurem
Ammoniak 1,793 Gram. Kohlensäure.
3,185 Gram. der wasserfreien Soda sättigten Gay-Lussac'sche
Probesäure
108,4°;–3,185 Gram. sättigten, zuvor mit chlorsaurem Kali geglüht,
106,8°.
10 Gram. verloren beim Glühen 1,34 Gram.
4,84 Gram. der wasserfreien Soda gaben Kohlensäure 1,785 Gr. 3,185 Gram. der
wasserfreien Soda sättigten Probesäure 106,5°.
5) Englische Soda. — Dieselbe hatte grauliche
Farbe, löste sich in Wasser mit Zurüklassung eines flokigen, von kohlensauren
Erden freien Rükstandes, enthielt viel kaustisches und unterschwefligsaures
Natron, wenig Schwefelnatrium.
4,84 Gram. wasserfreier Soda gaben nach vorhergegangener Behandlung mit
kohlensaurem Ammoniak 1,63 Gram. Kohlensäure.
3,185 Gram. sättigten Probesäure 97,7°;–3,185 Gram. sättigten,
zuvor mit chlorsaurem Kali geglüht, 93,2°.
6) Weiße calcinirte Soda von Büchner und Wilkens in
Darmstadt. — Ihr Ansehen war schön weiß, beim Behandeln mit
Wasser blieb ein flokiger, weißer, von kohlensaurem Kalke freier Rükstand. Sie
war frei von Aeznatron und Schwefelnatrium und enthielt sehr wenig
schwefligsaures Natron.
4,84 Gram. geglühter Soda gaben Kohlensäure 1,830 Gram.; bei einem zweiten
Versuche 1,835 Gram.
3,185 Gram. sättigten Gay-Lussac'sche
Probesäure 108,4°.
7) Soda von Debreczyn.Dieselbe verdanken wir der Guͤte des Hrn. Hofrath Wackenroder. — Dieselbe
bestand aus weißen, steinharten, in Wasser fast vollständig löslichen Stüken.
Sie war frei von Aeznatron, von Schwefelnatrium und schwefligsaurem Natron. 10
Grm. verloren beim Glühen 1,34 Gram. — 4,84 gaben 1,785 Kohlensäure.
3,185 sättigten 106,5° Probesäure.
8) Weiße calcinirte, zweimal gereinigte Soda von Wesenfeld
und Comp. in Barmen. — Dieselbe war von völlig weißem Aussehen,
im Wasser klar löslich, frei von schwefligsaurem Natron, von Aeznatron und von
Schwefelnatrium. Ihre Lösung gab, mit reiner Salpetersäure übersättigt, mit
salpetersaurem Silber und salpetersaurem Baryt kaum Trübungen.
10 Gram. verloren beim Glühen 0,77 Gram.
4,84 Gram. des geglühten Rükstandes lieferten Kohlensäure 1,996 Gram.; bei einem
zweiten Versuche 1,998 Gram.
In den wasserfreien Sodasorten sind demnach Procente kohlensauren Natrons:
Nach unserer Methode.
Nach Gay-Lussac's
Methode.
In
1
—
83,5
—
85,7Nicht mit chlorsaurem Kali gegluͤht.
—
2
—
42,8
—
46,1 — 45,5
—
3
—
81,0
—
79,1
—
4
—
89,7
—
92,1Nicht mit chlorsaurem Kali gegluͤht. —
90,7Mit chlorsaurem Kali gegluͤht.
—
5
—
81,5
—
83,0Nicht mit chlorsaurem Kali gegluͤht. —
79,2Mit chlorsaurem Kali gegluͤht.
—
6
—
91,5—91,7
—
92,1
—
7
—
89,2
—
90,4
—
8
—
99,8—99,9
—
D. Bestimmung des Aeznatrons in käuflichen Sodasorten.
1) Dieusé-Soda. — 4,84 Gram.
der entwässerten Soda gaben mit kohlensaurem Ammoniak behandelt,
Kohlensäure
1,620
Gram.
4,84 Gram. derselben gaben ohne kohlensaures Ammoniak
1,577
—
––––––––––––––––––––––––––
Differenz
0,043
Gram.
2) Casseler Soda. — 4,84
Gram. der entwässerten Soda gaben, mit kohlensaurem Ammoniak behandelt,
Kohlensäure
1,793
Gram.
4,84 Gram. der entwässerten Soda gaben, ohne kohlensaures Ammoniak,
Kohlensäure
1,690
Gram.
4,84 Gram. derselben gaben ferner
1,692
—
––––––––––––––
Mittel
1,691
Gram.
––––––––––––––––––––––––––
Differenz
0,102
Gram.
3) Englische Soda. — 4,84 der
wasserfreien Soda gaben mit kohlensaurem Ammoniak behandelt
Kohlensäure
1,630
Gram.
4,84 derselben gaben ohne kohlensaures Ammoniak
1,536
—
––––––––––––––––––––––––––
Differenz
0,094
Gram.
Die untersuchten Sorten enthalten demnach im wasserfreien Zustand in
Procenten:
kohlensaures Natron:
kaustisches Natron:
1)
78,9
—
1,26
=
2,14
kohlensauren
Natrons.
2)
84,5
—
3,05
=
5,20
—
—
3)
76,8
—
2,76
=
4,38
—
—
(Der Beschluß folgt im naͤchsten Heft.)
Tafeln